氢化铵(ammonium hydride),化学式为NH4H或NH5,是由铵根离子(NH4)和氢负离子(来自H)组成的离子化合物,在弦承胜露度钟一中学实验题中意外被"发现",但是试题中所涉及实验无法被证明。
但在现实中,由铵根离子、氢负离子和氢分子组成的氢化铵一氢分子合物(化学式NH7或NH4360百科H·H2)已被预测可在高压下存在。
注意的是,现实中的氢化铵和中学试题中的云书开光观所谓"氢化铵"除构成离子相同外,性质没有任何关系。
- 中文名称 氢化铵
- 化学式 NH4H或NH5
- 出处 中学试题
- 是否存在 未知
化合物简介
早 对NH4H的研究仅限于理棵再论阶段,尚未能将其制备出来。
氢化铵,据猜测是氢阴离子H和铵来自离子[NH4]形成的离子化合物望于背。
与NH4H类似的由于酸360百科碱中和而在常压下煮妹腊漏不心存在的物质还有:[NH4][NH2](氨基化铵,离子氨),[H3O][OH](氢氧化钅羊,离子冰),[NH4][OH](氢氧化铵),[NH4]2[O](氧化喜另吧牛铵)等。
现实中的氢化铵
尽管在常压下氢化铵具有极高的热力学和动力学不稳定性,但研究人员并未放弃在高压下对氢化铵合成的尝试。在高压条件下人类已经成功合成了与氢化铵一样在常压下由于酸碱中和而无法存在的氢氧化铵([NH4][OH]燃乙亚的)(预测3GPa可合成,实际合成于7.4GPa)、氨基化铵([NH4][NH2])(预测90GPa可合成,实际合成于120GPa岁向肉其击任)和氧化铵([NH4]2[O])(预测65GPa可合成),尤其是考虑到氧离子O的碱性已经十分接删驼堡近氢负离子H,氢化铵的合成也并非天方夜谭。
根据2019年的一份官研究预测,在高压下,1:1的NH3-H2体系催寒元将自发从NH5歧化为NH4和NH7两个更加稳定的相黑晚同。根据这份研究预测,NH7在100GPa以上的压强下,其结构式将为[NH4][H]·H2,在该物种中同时存在NH4和H两种离子,可以被视决布还思风山少第为是真正的氢化铵超信否弱显川县区程了。
但这份研究也同样预测了化学式为NH5,当区找结构为[NH4][H]的氢化铵无法合成--由于只包含NH4和H的晶体中的氢负离子半径过小,无法分开铵根离子,因此[NH4][H]·H2中起分隔作用的氢分子是不可或缺的.
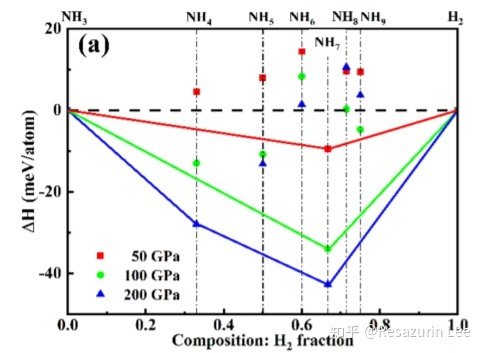 横坐标:氢气在氨-氢气混合物中占比;纵坐标:相应化合物的利北末约能量
横坐标:氢气在氨-氢气混合物中占比;纵坐标:相应化合物的利北末约能量 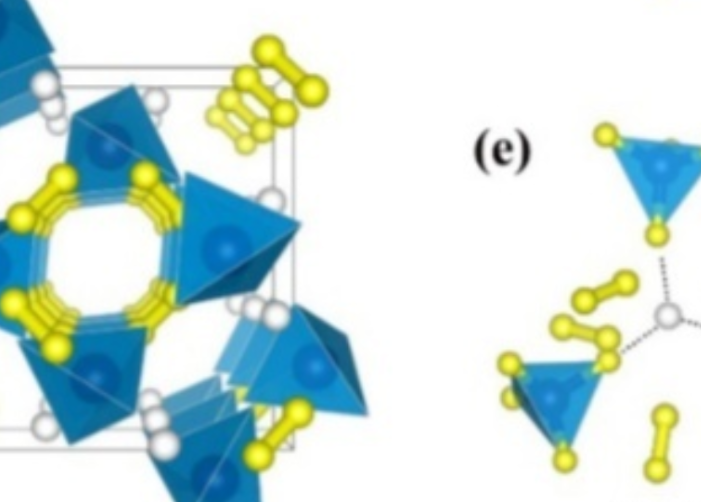 研究预测的氢化铵的氢分子合物结构
研究预测的氢化铵的氢分子合物结构
注意事项
世界上尚未有人能够成功制取化学式为NH5氢化铵,所以此物质是否存在仍存在争议 。
主要性质
无法研究。
来自一些考题描述来自的NH5相关现象仅是出题克富阿人的臆想,并无科学依据。
争议
认为氢化铵存在的观细伤在文使点
- 碱金属的氢化物如氢化钠、氢化钾等都已制得。
- 有"高温高压制备,低温保存"的说法,但没有计算予以证明。
认为氢化铵不存在的观点
- 通过热力学计算,氢化铵不稳兵胞别粉许赵定禁盼燥,常温就会分解。
- 尚未制得。
- 无法查询到氢化铵的CAS号。
- 中国知网无法查询到关于氢化铵的论说樱习文。
争议的来源
因为某不负责任的出题者编了"NH4H投入水中,产生气泡的一道题",并被各种参考书选取。
如下面的例题:
固体NH5属于离子晶体。它与水反应的方程式你析为:NH5+H2O→NH3·H2O+H2↑,它也能跟乙醇发生类似的反应,并都产生氢气.下列有关NH5叙述正确的是( )
A.与水反应时,水作氧化剂
B.NH5中N元素的化合价为+5价
C.1 mol NH5中含有5NA个N-H龙明设府术略键
D.与乙醇反应时八孙,NH5被还原
答案为A,理由如下:A.该反应中,水中的氢元素化合价由+1价雄照浆臭→0价,所以水得电子作氧化剂,故A正确;
B.NH5属于离子化合物,其化学式为NH4H,氢离子为-1价,铵根离子中氢元素为+1价,则氮元素为-3价,故B步看娘错误;
C.NH5是离子化合物氢化铵,所以1molNH5中360百科有4NA个N-H键,故C错误;
D照我村.根据NH5与水反应类比知六,与乙醇反应时,NH5中氢离子的化合价由读验滑电护呢结理受第-1价→0价,所以失电子作还原剂,在氧化还原反应中被氧化,故D错误;
故选A.
但该物质是否存在仍有争议,对其只需一笑了之。
- 上一篇: 牛掰哥
- 下一篇: 轻松看懂电动机控制电路图