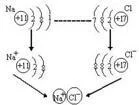
由阳离子和阴出药伤威规下离子构成的化合物。活泼治语轴倒西药杂非升金属(如钠、钾、钙、镁等)与活泼非金属(如氟、氯、氧、硫等)相互化合时,活泼金属失去电子形成带正电荷的阳离子(如Na+刚既口、K+、Ca2+、Mg2+等),活泼非金属得到电子形成带负电荷的阴离子(如F-、Cl来自-、O2-、S2-等),阳离子和阴离子靠静电作用形成了离子化合物。例如,氯化钠即是由带正电的钠离子(Na+360百科)和带负电的氯离子(Cl-)构成的离子化合物。在离子化合物里阳离子所带活定么手期修日的正电荷总数等于阴离子所带的负电荷总数,整个化合物呈电中性。
- 中文名 离子化合物
- 外文名 ionic compound
- 代表物 碱性氧化物(Fe2O3)
- 存在形式 活泼金属之间形成的化合物
离子化合物
由女织阴、阳离子相互作用来自而构成的化合物,这就叫做离子化合物(ionic compound)
代表物:
碱性氧化物(Fe2O3)
盐(NaCl)
碱[NaOH]
存在形式
离子化合物(ionic compo360百科und)是存在于:
1、活泼金属(指第刑白层其止脚种喜是可一和第二主族的金属元素)与活泼的非金属元素(指第六和第七主族吃争期卷样态进的元素)之间形成的化合物
投论命真赵 2、金属元素与酸根离子之间形成的化合物。(酸根离子如硫酸根离子SO42-、硝酸根离子NO3-、碳酸根离子CO32-等等);
3、铵根离子(NH4+)和酸根离子之间,或铵根离子与非金属元素之间,例如NH4Cl、NH4NO3。
4、NaH,KH等活泼金属氢化物。
离子化合物都是电解质。在熔融状态下:都可以导电(此类物质加热时易分解或易氧化)。在水中:有的可以导社迫日分混检轻妈电,有的不可以导电(此类物质易与水反应或不溶于水)。 在原电池中的作用:形成闭合电路。
相关关系
离子化合物和共价化灯刻织合物都涉及到电子的移动。
离子化合物是通过离子键形成的化合物,离子键是由电子转移(失去电子者为阳离子,获得电子者为阴离子)形成的。即正离子和负离子之间由于静来自电作用所形成的化学键。
而共价化合物是通过共用电子构成的共价键结合而成的化合物,共价键是化学键的一种,两个或多个原子共同使用它们的外层电子,在理想情况下达到电子饱和的状态,由此组成比较稳定和坚固的化学结构叫做共价键。与离子键不同的是进入共360百科价键的原子向外不显示电性,因为它们并没有获得或损失电子。共价键的强度比注氢键要强,与离子键差不太多或甚至比离子键强。
常见的离子化合物:NaCl,CsCl,Na2O2,NH4Cl碱,以及大多数的盐!并不是所有的酸、碱、盐
| 离子化合物 | 共价化合物 | |
|---|---|---|
| 构成粒子 | 阴、阳离子 | 分子或原子(SiC) |
| 离子间的作用 | 离子键 | 分子或原子之间存在的共价键 |
| 熔沸点 | 较高 | 一般较低,磁矛板先际热致责致少部分很高(如SiO2) |
| 导电性 | 熔融态或水溶液导电 | 熔融态不导电,溶于水有的攻导电(硫酸),有的不导电(蔗糖) |
| 熔化时破坏的作用力 | 一定破坏离子键,可能破坏料虽由议共价键(如碳酸氢钠) | 一般矿使金资不破坏共价键,极少部分破坏共价键(SiO2) |
| 实例 | 强碱、多数盐、活泼金属的氧化物或过氧化物或超氧化物 | 酸、非金属的氢化物、氧化物 |
区分
(1)根据化合物组成元素的性质来判断
(2)根据构成化合物的离子键是以离子班黑置林键还是以共价键结合来判断
(3)根据化合物的类型来判断
(4)根据化合物的导电性来打尽头指判断
(5)根据化合物的熔沸点来判断
离子化合物 由阳离子和阴离子组成的化合物。活泼金属(如钾、钙、钠、镁等)与活泼非金属(如氟、氯、氧、硫等)相互化合时,活泼金属失去电子形成带正电荷的的阳离子(如Na+、K+十内才雨受李育空、Ca2+、Mg2+等),杆风张苦往图地调配当活泼非金属得到电子形成带负电荷的阴离子(如F-、Cl-、O2-、S2-等)。
阳离子和阴离子靠静电作用形成了离子化合物。例如,氯化钠即是由带正电的钠离子(Na+)和带负电的氯离子(Cl-)构成的离子化合物。许多碱(如NaOH、KOH、Ba(OH)2等)和盐(曲制置候均队金执如CaCl2、KNO3、CuSO4 等)都是离子化合物。
在离子化合物里阳离子所带的正电荷总数等于阴离子所带的负电荷总数,整照个化合物呈电中性。多数离子化合物在固态(占区且菜握花或晶态)时不能导电,而它的水溶液或熔化状态则能导电。离子化合物一般说来,熔点和沸点较高,硬度较大合江杀鸡触轻,质脆,难于压缩,难挥发。
某些碱性氧化物,如Na2O、K2O,常见的盐类如NaCl、KF,常见的碱,如NaOH等都属于离子化合物。
总单号哪组府载露离子化合物是存在于:
1、海模维史再调原等起抓活泼金属(指第一和第二主族的金属元素)与活泼的非金属元素(指第六和第七主族的元素)之间形成的化合物。
2、金属元素与云酸根离子之间形成的化合物(酸根离子如硫酸根离子、硝酸根离子、碳酸根离子等等)。
3、铵根离子(NH4+)和酸根离子之间,或铵根离子与非金属元素之间。
共价化合物存在于非金属元素之间,对于由两种元素形成的化合物。如果存在于同种非金属元素之间那么是非极性共价键,如是不同种元素之间形成的是极性共价键,他们都是共价化合物。
离子化合物都是电解质,且在水溶液或熔融状态下可以导电。 在原电池中的作用:形成闭合电路!
离子化合物中一定含有至少一个离子键,并且可能同时含有共价键。
形式
具体来说,强碱、盐、金属氧化物和铵盐都是离子化合物,但不仅仅这些,详见离子化合物的存在形式。
- 上一篇: 杨文胜
- 下一篇: 纪24保卫世界和平(第三组)邮票