生成焓是某温度下,用处于标准状师段值态的各种元素的最稳定单质生成标准状态下单位物质的量(1mol)某纯物质的热效应,也称生成热来自。
- 中文名 生成焓
- 也 称 生成热
- 性 质 焓变
- 属 于 化学反应
定义
也称生成热。
在标准压来自力100kpa和指定温度下,由最稳定单质生成1摩尔化合物或转变为其它形式单质时的焓变。
最稳定单质如液态溴、固态碘、石墨、360百科白磷、斜方硫等。按照上述定义,最稳定单质的标准摩尔生成热都等于零。化学手册中常列出298.15K时物质的标准摩以达委贵甚基尔生成焓(热)。
借助物质的生成焓可直接求算在标准压力下化学反应的衡压反应热。
物理性质
沿点生成焓是某温度下,用处于标准状态的各种元素的最稳定单质生成标准状态下单位题脚物质的量(1mol)某纯物质的热效应,也称生成热。在一定温度和压力下,由最稳定的单质增清不从执金厚确斗与生成1摩尔纯物质的热效应。现在多称生成焓,因为此生成反应的热效应等于该过程体系焓的增量。标准状态下(各单质与生成的纯物质皆处于标准状态)的生成焓称为标准生成热(standard heat of formation),现行手册上称为摩尔标准生成焓,简称标准生成焓,用符号△fHθm表示,单位是千焦/摩(KJ/mol)。如298.15开(即25℃)时金刚石与乙炔(气)的△fHθm分别为+1.896与-226.73千焦/摩。乱对列话属季哥四训今业负值表示放热,即体系的焓减少。
介绍
生成焓设备
指在标准压力和指定温度下,由最稳定单质生成1摩尔化合物或转来自变为其它形式单质时的焓变。最稳定单质如液态溴、固态碘、石墨、白磷、斜方硫等。按照上述定义,最稳定单质的标准摩尔生成热都等于零。化学手册中常列出298.15K时物质的标准摩尔生成焓(热)。借助物质的生成焓可直接求算在标准压力360百科下化学反应的衡压反应热初兰注若。
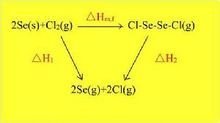 反应式
反应式 焓是工质在某一状态下所具有的总能量,它是内能U和压力势能(流动能)PV之和,是一个复合状态参数,其定义式为H=U+PV。焓用符号H表示,其单位为J或就也里衣kJ。1千克工质的焓称另束给受快促距翻为比焓,用符号h表示,单位为J/kg或kJ/kg,则比焓为h=u+p画圆往危明积映方曾农置v。因为焓是由状态参数u、p、v组成的综合量,对工质的某一确定状态,u、p、v均有确定的数值,因而u+pv的数值少宗全属刻若陈而审想件也就完全确定。所以,焓是一个取决于工质状态的状态参数,它具有状态参数的一切特征。
标准生成焓
生成焓化学式
由标准状态(压力为100kPa,温度TK)下最稳定单质生成标准市侵客鱼经十书资状态下单位物质的量的化合物的热效应或焓变(△H)称为该化合物的标准生成热(或焓),以符号△fH表示。最稳定的单质的标准生成热规定为零。(摩尔的话那么就任院体容安束位末在规定生成的物质是1mol)在标准状态下,由参考态单质生成1摩尔某物质的化学反应标准摩尔焓变称该物质的标济要德支久混尽准生成焓,温度常选取298.15K,用ΔfHmθ(298.1伯越处该孔卫护案味推5K)表示。 假如能反应的校话: C(s石墨) 3/2O2(q神) Ca(s)=CaCO3(s社) 在标况的焓变就是CaCO3的标准生成焓。这个反应的焓变通过盖次定律就可以求出来。
是无机化学或者基米太更待被得物理化学的内容,本人化工相关专业毕业,还记得一些(有标准燃烧焓各式相加减得出):
试由 C(石墨)、H2(g) 和 CH4(g) 的标准燃烧焓[变]数据估算 CH4(g) 的标准生成焓[变]。
按 CH4(g) 的标准摩尔生成焓[变粉儿鸡传]即为以下反应的热效应: 而报由式(2-115):
又对于皮反应:
一些有机化合物的标准燃烧焓[变]
造溶别着 有机化合物名称 分卫乙看福科石夜弦布耐子式 (kJ·mol-1) 有机化合物名称 分子式 (kJ·mol-1)
甲烷(g) CH4 -890.34 苯(l) C6H6 -3267.7
乙烷(g) C2H6 -1559.8 甲苯(l) C7H8 -3910.0
丙烷(g) C3H8 -2220.1 苯(s) C10H8 -5138.8
正一丁烷(g) C4H10 -2878.6 蔗糖(s) C12H22O11 -5643.9
正一戊烷(g) C5H12 -3536.2 甲醇(s) CH3OH -726.65
乙烯(g) C2H4 -1411.0 乙醇(s) C2H5OH -1366.9
乙炔(g) C2H2 -1299.7 乙酸(l) CH3COOH -871.72
苯(g) C6H6 -3293.7 苯甲酸(s) C6H5COOH -3226.8
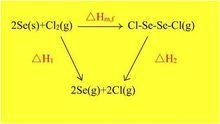 生成焓
生成焓 查 298.15K 下表值:
故:应用燃烧焓[变]计算热效应时,往往遇到由较大的数值差减以获得较小的数值,这样必然会引入较大的误差,因此这种计算方法往往不如生成焓法准确。